视频1
视频2
三、超声内镜下的直肠癌分期
直肠癌是消化系统常见的恶性肿瘤,随着内窥镜及影像技术的发展,其诊断已不是难题。早期直肠癌只需行内镜或手术治疗,而进展期患者(T3-4,N0 或者 TX,N1-2)术前建议新辅助放化疗。新辅助放化疗能减少肿瘤的体积、辅助保肛、提高完整切除和降低局部复发率,因此,直肠癌术前精确分期对患者个体化治疗是非常重要。
目前,临床上用于直肠癌术前分期方法有 CT、MRI和超声内镜。CT 对于明确直肠癌的远处转移是首选的方案,但其对于局部T分期价值不大。2018年NCCN指南推荐 MRI为直肠癌术前T分期的首选方法,但有幽闭恐惧症及体内有金属支架的患者无法适用,且它对T2及以下分期准确度欠佳。超声内镜可通过直肠腔内注水清晰肠壁层次,对于肿瘤局部浸润有较好的成像,近年多项研究表明EUS与MRI在T2、T3中具有相似的准确度,对于T2及以下分期更具有优势。
超声内镜下直肠壁可分为五层结构,分别为高(粘膜浅层)、低(粘膜深层及肌粘膜层)、高(粘膜下层)、低(固有肌层)、高回声(浆膜层和直肠周围脂肪)(加一张分层图),直肠癌超声下表现为局部正常肠壁结构中段或消失,代之为低回声病变。EUS下的肿瘤T分期具体如(图5)。
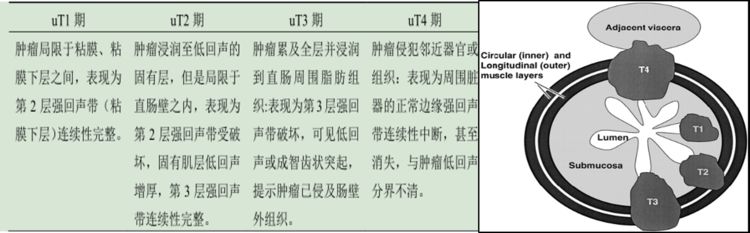
图5:直肠癌超声下T分期
下面通过几个典型的病例分享下各期直肠癌超声下的典型特征。
(一)uT1期直肠癌
病例一:患者便血完善肠镜检查,发现直肠见菜花样新生物,病灶中央凹陷,局部糜烂,超声内镜下见粘膜层明显增厚,第二层高回声带(粘膜下层)连续性完整(图6),动态视频中似乎看到病灶中央部分有粘膜下层缺损,彩色多普勒显示为较粗滋养血管(视频 3),术后病理证实病灶限于粘膜层及粘膜下层。
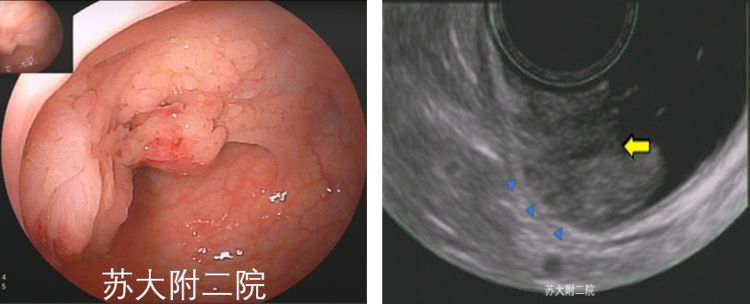
图6:a肠镜下表现 b EUS显示粘膜下层完整(蓝色箭头)
视频3
(二)uT2期直肠癌
老年男性,肠镜提示直肠增生性病灶,CT提示直肠癌,未见远处转移,术前完善EUS,超声下见局部病灶处肠壁正常结构消失,病灶最深处累及固有肌层,而浆膜层或其与周围组织的高回声带尚完整连续(图7,红色箭头),诊断为直肠癌(uT2期),术后病理证实为绒毛状管状腺瘤伴局灶癌变,浸润固有肌层。
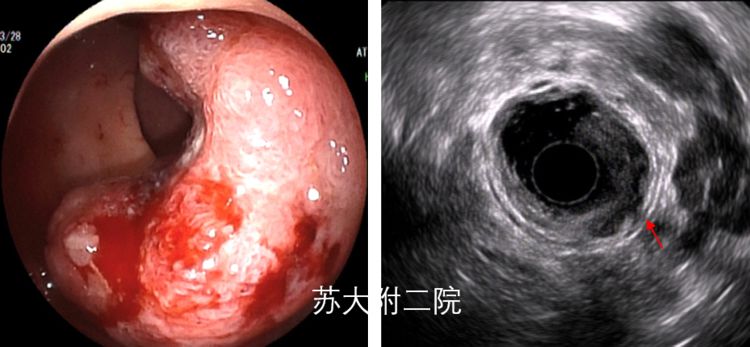
图7:a白光下表现 b超声声像,红色箭头所示外膜完整
(三)uT3期直肠癌
uT3 期直肠癌表现为肿瘤累及全层并浸润到直肠周围组织,但未累及周边脏器,在EUS下表现为浆膜层突破或其与周围组织的高回声带中断,伴或不伴周边淋巴结转移(图8-10及视频4)。
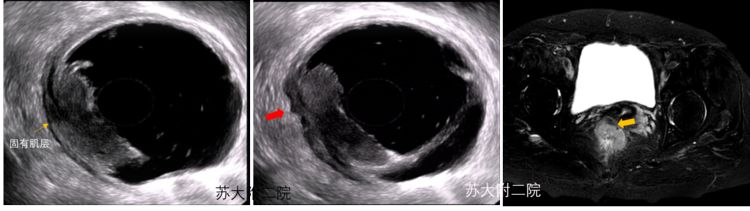
图8:a示肿块大部分区域外膜完整 b其中局部区域呈齿突样改变(红色箭头处)未累及周边组织,诊断为T3期 c 磁共振下提示侵犯固有肌层外脂肪组织
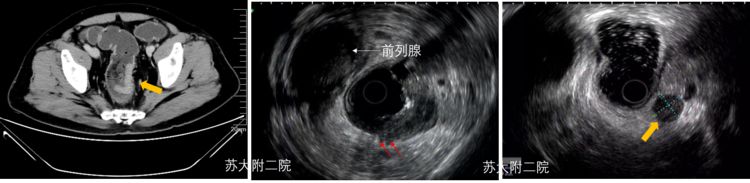
图9:a CT提示直肠下端癌 b EUS下可见局部病灶外膜层完整性破坏,呈齿突状改变(红色箭头)c 直肠外见低回声类圆形淋巴结
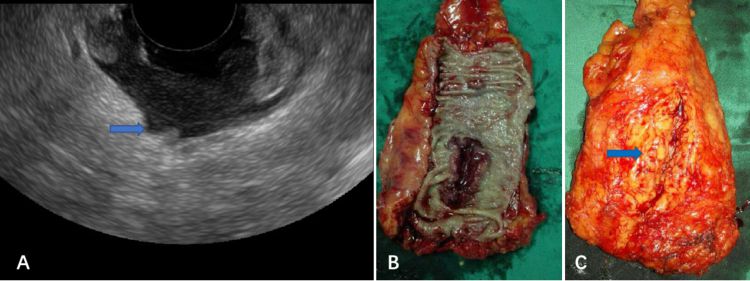
图10:A EUS见病灶呈锯齿状突破浆膜层(蓝箭头) B 大体标本粘膜侧 C 大体标本浆膜侧(蓝箭头见病灶突破处)
视频4
(四)uT4期直肠癌
uT4 期直肠癌主要诊断依据为病灶突破浆膜层并侵犯邻近器官(生殖系统或泌尿系统)(图11及视频5),部分晚期直肠癌病灶外见腹水(图12)。
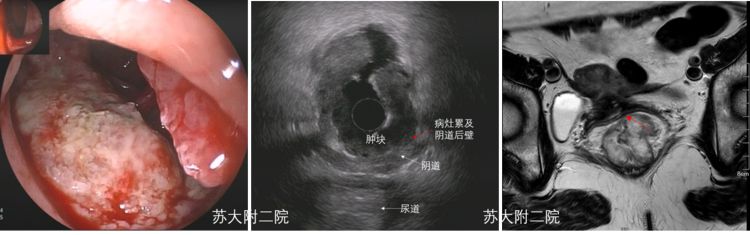
图11:a白光下直肠见浸润性病灶 b EUS下病灶累及引导后壁 c 磁共振显示病灶与阴道后壁界限欠清
视频5
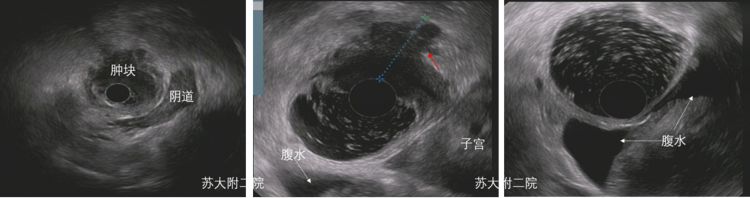
图12:a、b提示直肠右后壁局部正常肠壁结构消失,代之以低回声病灶,病灶累及邻近组织(红色箭头) c 病灶外见无回声腹水形成
(五)EUS对直肠癌新辅助放化疗后再分期
术前放、化疗已是局部晚期直肠癌的标准方案。大量临床研究证实新辅助放化疗能有助保肛、提高完整切除和降低局部复发率,但如何评估新辅助放化疗的效果,临床尚无共识手段,EUS应有一席之地,下面患者诊断时EUS显示病灶巨大,在新辅助质量后复查病灶明显缩小,最终成功手术保肛。
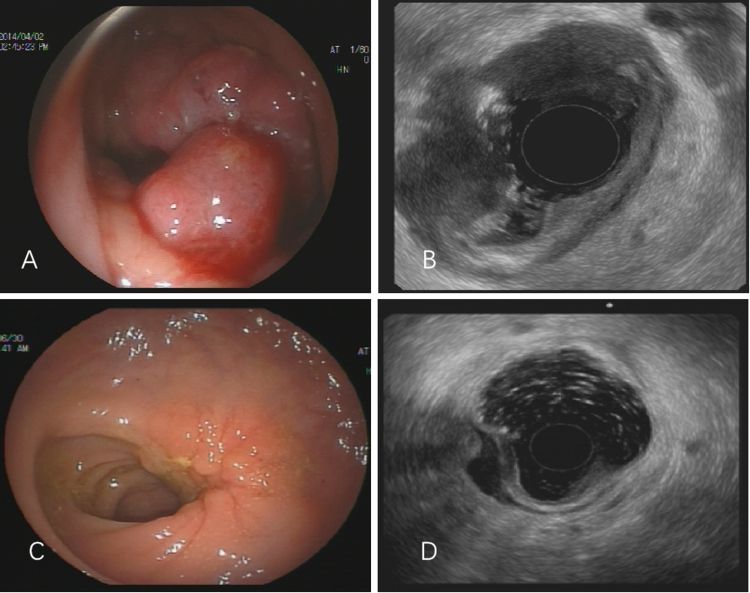
图13:A-B 初诊时病灶巨大且距肛门4厘米,手术无法保肛C-D 标准新辅助放化疗后病灶明显变小,成功保肛
近年来,超声内镜设备普及率逐年增高,但很多单位仅将其放在上消化道和胆胰疾病的诊治,其实,EUS在纵隔、盆腔邻域也有很好的表现。盆腔和直肠疾病众多,EUS尤有用武之地,本期内容介绍了盆腔探查策略和直肠癌的EUS分期,希望对大家有所帮助,下一期我们将带给大家EUS对直肠癌术后复发的监测价值。
程桂莲 徐丽明 吴伟 胡端敏
苏州大学附属第二医院消化科
当下,超声内镜(EUS)主要用于上消化道及胆、胰探查。对于直肠及盆腔病变,仅作为其他影像工具(如CT和MRI)的补充。但就我们的经验而言,EUS不仅直视肠腔、还能注水延展肠壁,对直肠癌的分期、浆膜侧复发等有一定优势。接下来,我们将分三期介绍EUS在直肠和盆腔中的应用,本次带来的是盆腔探查策略和直肠癌分期。
一、内镜、EUS和CT/MRI的协同对应
直肠及周边结构探查时,EUS术者需参照内镜和超声图像,但两视野中的直肠四壁指向不一,有时甚至相反,这让初学者往往无所适从。因此,探查前,首先要让内镜和超声视野的方向协同一致。因EUS图像可被翻转和旋转处理,故笔者以肠镜视野为标准来调整超声,左侧卧位是标准体位,此时,肠镜自然状态下的视野指向是:屏幕上方---直肠后壁、屏幕下方---直肠前壁、屏幕左侧---直肠左侧壁、屏幕右侧---直肠右侧壁(图1 A)。我们按上述方位来调节EUS图像,EUS图像默认为口侧向肛侧的远测观,这和肠镜视野相反,我们先通过F1键(FUJIFILM SU-9000)将EUS断面改为肛侧向口侧的近侧观(图 2),随后,因重要盆腔脏器(膀胱、前列腺、精囊腺、子宫等)均位于直肠前方,故我们将这些结构调至屏幕6点位(因内镜6点位对应前壁),这样,内镜和EUS视野方向一致(图1 B)。此外,EUS探查盆腔常需参考CT/MRI断面(图1 C),我们只要简单的将CT/MRI片子旋转180°即可对应超声图像(图1 D)。通过以上调整,我们实现了内镜视野,超声图像和CT/MRI的协同一致。
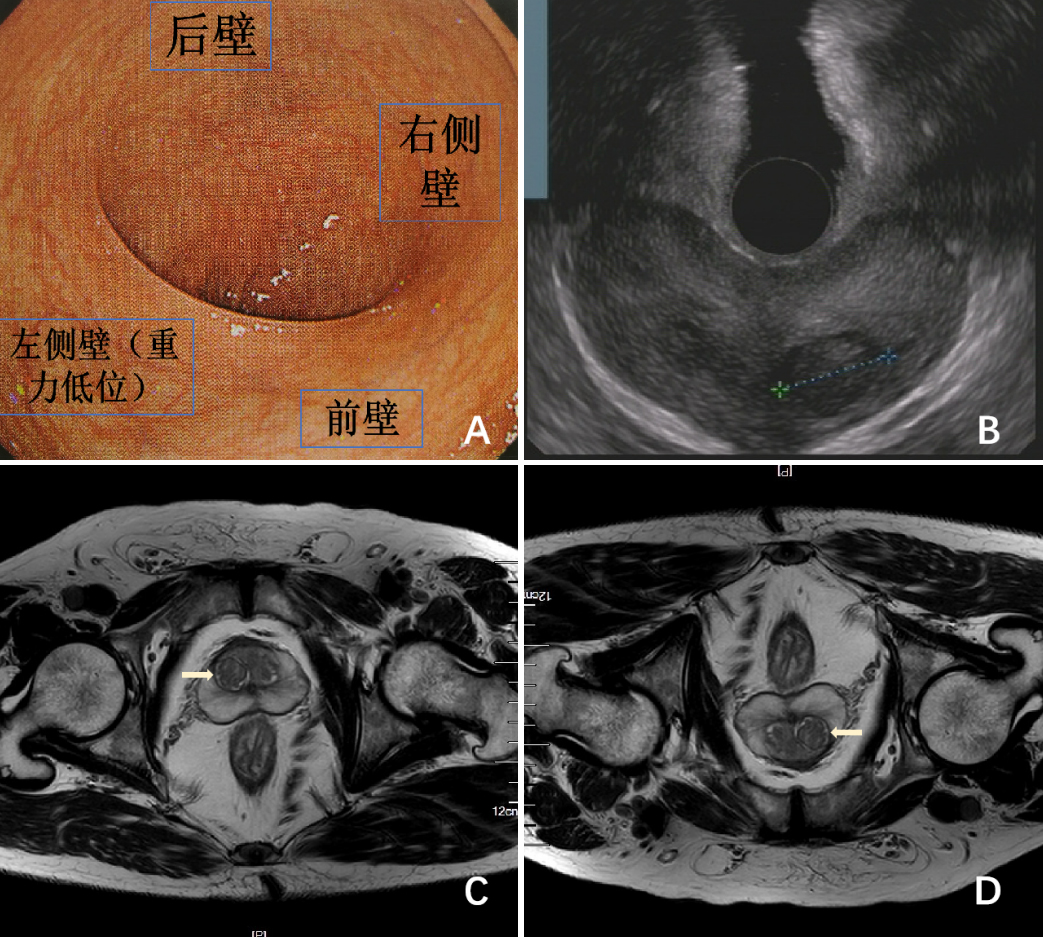
图1:内镜、EUS和CT/MRI的协同对应(黄色箭头为右侧前列腺结节)
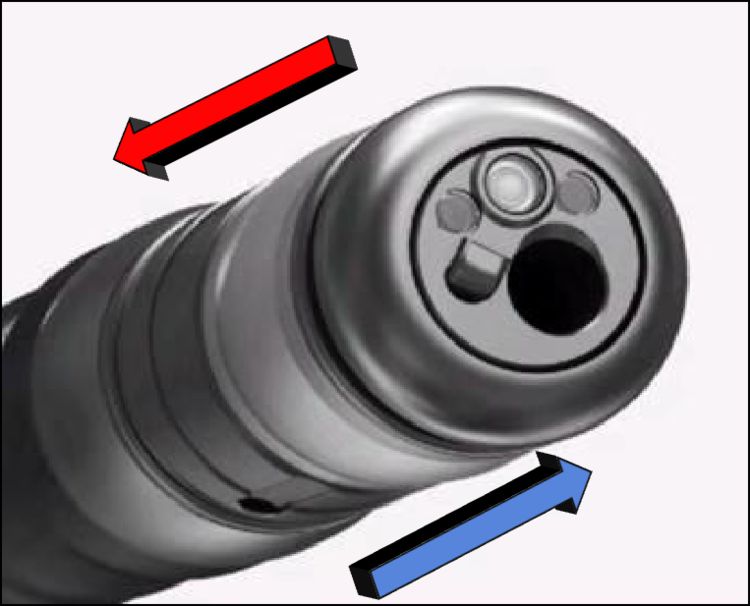
图2:红箭头代表EUS成像远测观(默认设置),蓝箭头为近侧观
二、超声内镜盆腔探查技巧
超声内镜探查盆腔时,男、女性患者因生理结构不同存在差异。但不管男女,由于直肠位于盆腔后侧,所有盆腔内重要结构均位于直肠的前侧壁(图3)。超声内镜探查过程中因肠腔弯曲,往往需要旋转镜身,这必然会导致超声影像和千变万化,方向丢失。
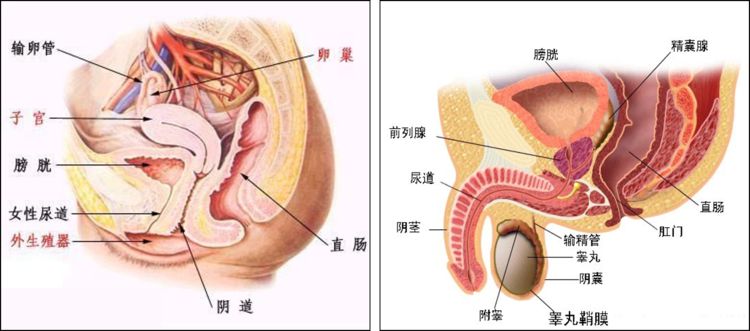
图3:盆腔的结构矢状位图(左为女性,右位男性)
笔者在此介绍两种盆腔探查方法:1、退镜法:左侧卧位直接进镜至直乙交界(约距肛门12cm左右),吸气冲水,肠腔外可发现无回声袋状结构(膀胱声像),近侧观成像下将膀胱旋转至6点方向。我们亦可借助肠腔内液体或气泡来确认EUS影像是否调节到位(左侧卧位,由于重力作用,超声视野下气泡处为肠壁右侧,反之积水位于左侧),确定方位后逐步退镜观察相应结构。退镜法过程中无阻力,但当患者排尿后,找寻膀胱等路标结构会有困难。2、进镜法:将超声肠镜置于肛缘,即可清晰观察到肛管的三层超声结构,分别为粘膜层、肛门内括约肌及肛门外括约肌。继续进镜,男性可相继观察到尿道、前列腺、精囊、膀胱及髂内血管;女性则相继观察到阴道、子宫、附件及尿道、膀胱,其中阴道子宫靠近探头。进镜法相对于退镜法而言,无需先识别膀胱等结构,直接从肛门开始探查,但因在没有内镜视野下进镜,有时阻力明显。(图4及视频1、2)。
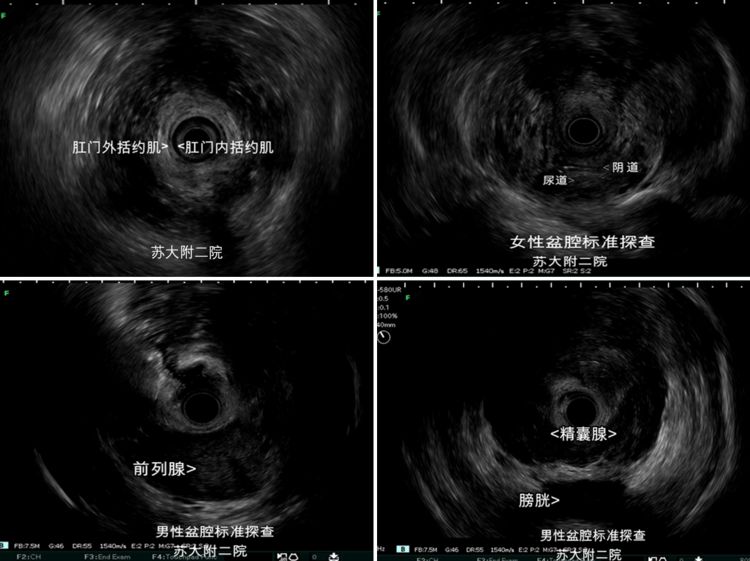
图4:盆腔环扫超声内镜结构图
视频1
视频2
三、超声内镜下的直肠癌分期
直肠癌是消化系统常见的恶性肿瘤,随着内窥镜及影像技术的发展,其诊断已不是难题。早期直肠癌只需行内镜或手术治疗,而进展期患者(T3-4,N0 或者 TX,N1-2)术前建议新辅助放化疗。新辅助放化疗能减少肿瘤的体积、辅助保肛、提高完整切除和降低局部复发率,因此,直肠癌术前精确分期对患者个体化治疗是非常重要。
目前,临床上用于直肠癌术前分期方法有 CT、MRI和超声内镜。CT 对于明确直肠癌的远处转移是首选的方案,但其对于局部T分期价值不大。2018年NCCN指南推荐 MRI为直肠癌术前T分期的首选方法,但有幽闭恐惧症及体内有金属支架的患者无法适用,且它对T2及以下分期准确度欠佳。超声内镜可通过直肠腔内注水清晰肠壁层次,对于肿瘤局部浸润有较好的成像,近年多项研究表明EUS与MRI在T2、T3中具有相似的准确度,对于T2及以下分期更具有优势。
超声内镜下直肠壁可分为五层结构,分别为高(粘膜浅层)、低(粘膜深层及肌粘膜层)、高(粘膜下层)、低(固有肌层)、高回声(浆膜层和直肠周围脂肪)(加一张分层图),直肠癌超声下表现为局部正常肠壁结构中段或消失,代之为低回声病变。EUS下的肿瘤T分期具体如(图5)。

图5:直肠癌超声下T分期
下面通过几个典型的病例分享下各期直肠癌超声下的典型特征。
(一)uT1期直肠癌
病例一:患者便血完善肠镜检查,发现直肠见菜花样新生物,病灶中央凹陷,局部糜烂,超声内镜下见粘膜层明显增厚,第二层高回声带(粘膜下层)连续性完整(图6),动态视频中似乎看到病灶中央部分有粘膜下层缺损,彩色多普勒显示为较粗滋养血管(视频 3),术后病理证实病灶限于粘膜层及粘膜下层。

图6:a肠镜下表现 b EUS显示粘膜下层完整(蓝色箭头)
视频3
(二)uT2期直肠癌
老年男性,肠镜提示直肠增生性病灶,CT提示直肠癌,未见远处转移,术前完善EUS,超声下见局部病灶处肠壁正常结构消失,病灶最深处累及固有肌层,而浆膜层或其与周围组织的高回声带尚完整连续(图7,红色箭头),诊断为直肠癌(uT2期),术后病理证实为绒毛状管状腺瘤伴局灶癌变,浸润固有肌层。

图7:a白光下表现 b超声声像,红色箭头所示外膜完整
(三)uT3期直肠癌
uT3 期直肠癌表现为肿瘤累及全层并浸润到直肠周围组织,但未累及周边脏器,在EUS下表现为浆膜层突破或其与周围组织的高回声带中断,伴或不伴周边淋巴结转移(图8-10及视频4)。

图8:a示肿块大部分区域外膜完整 b其中局部区域呈齿突样改变(红色箭头处)未累及周边组织,诊断为T3期 c 磁共振下提示侵犯固有肌层外脂肪组织

图9:a CT提示直肠下端癌 b EUS下可见局部病灶外膜层完整性破坏,呈齿突状改变(红色箭头)c 直肠外见低回声类圆形淋巴结

图10:A EUS见病灶呈锯齿状突破浆膜层(蓝箭头) B 大体标本粘膜侧 C 大体标本浆膜侧(蓝箭头见病灶突破处)
视频4
(四)uT4期直肠癌
uT4 期直肠癌主要诊断依据为病灶突破浆膜层并侵犯邻近器官(生殖系统或泌尿系统)(图11及视频5),部分晚期直肠癌病灶外见腹水(图12)。

图11:a白光下直肠见浸润性病灶 b EUS下病灶累及引导后壁 c 磁共振显示病灶与阴道后壁界限欠清
视频5

图12:a、b提示直肠右后壁局部正常肠壁结构消失,代之以低回声病灶,病灶累及邻近组织(红色箭头) c 病灶外见无回声腹水形成
(五)EUS对直肠癌新辅助放化疗后再分期
术前放、化疗已是局部晚期直肠癌的标准方案。大量临床研究证实新辅助放化疗能有助保肛、提高完整切除和降低局部复发率,但如何评估新辅助放化疗的效果,临床尚无共识手段,EUS应有一席之地,下面患者诊断时EUS显示病灶巨大,在新辅助质量后复查病灶明显缩小,最终成功手术保肛。

图13:A-B 初诊时病灶巨大且距肛门4厘米,手术无法保肛C-D 标准新辅助放化疗后病灶明显变小,成功保肛
近年来,超声内镜设备普及率逐年增高,但很多单位仅将其放在上消化道和胆胰疾病的诊治,其实,EUS在纵隔、盆腔邻域也有很好的表现。盆腔和直肠疾病众多,EUS尤有用武之地,本期内容介绍了盆腔探查策略和直肠癌的EUS分期,希望对大家有所帮助,下一期我们将带给大家EUS对直肠癌术后复发的监测价值。