
*以下内容中所有出现的LCI指联动成像技术(LCI:Linked Color Imaging);BLI指蓝光成像技术(BLI:Blue Light Imaging)
本期讲座,丁伟群教授分别从以下几个方面讲解了同时性多发性早期胃癌:
- 定义
- 主病灶和副病灶特征分析
- 高危人群和危险因素
- 如何避免ESD术前精查漏诊
- 治疗策略
*以下内容为部分摘要,完整内容敬请点击视频观看
华山医院的案例
教授首先介绍了来自华山医院的两个典型病例
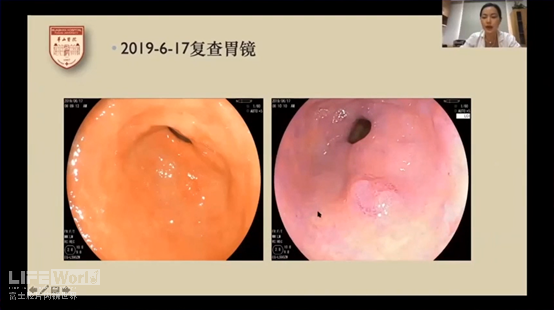
胃镜检查时在胃窦大弯处发现病灶,丁教授表示与白光相比,LCI模式可以更明确的看到病灶。
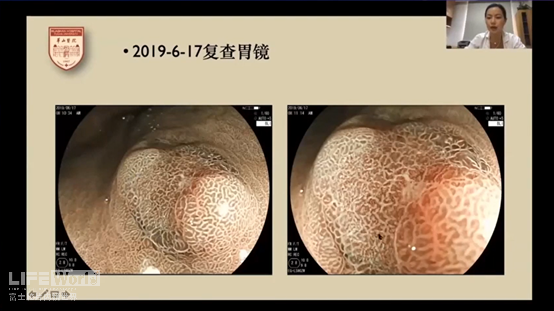
对病变进行BLI放大观察后,可看到病变中央凹陷处腺体略微紊乱,后续执行ESD治疗,病理显示为低级别上皮内瘤变。
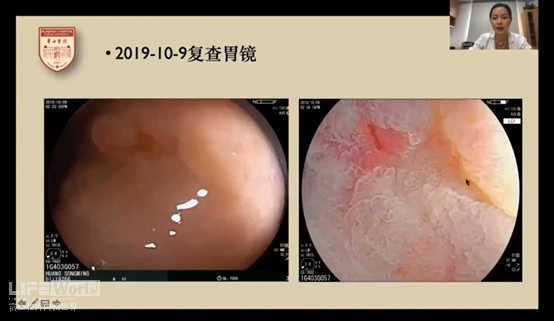
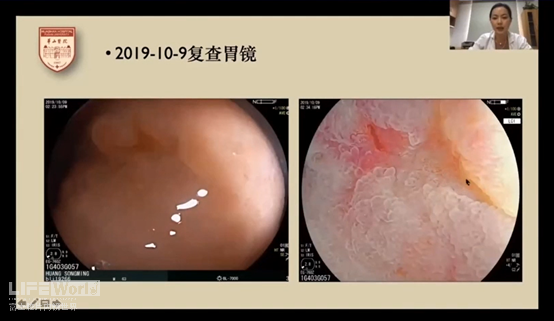
三个月后病人复查,在胃窦小弯侧再次发现病灶,BLI放大观察后可看到腺体不规则或消失,操作ESD后病理提示为中分化腺癌。
同时性多发性早期胃癌的定义
丁教授经过文献解析,将定义概括为:
同时性多发早期胃癌(synchronous multiple early gastric cancer:SMEGC)指在胃内不同部位同时或一定期间内出现的2个及以上相互独立的肿瘤,每个病灶均经病理确诊为恶性。各癌灶间彼此孤立,组织学上有正常胃黏膜组织间隔,详细检查后严格排除系癌灶间互为转移[1]。
主病灶和副病灶特征分析
丁教授经过文献解析[2],将主副病灶特征概括为:
1) 第一次ESD发现的病为主病灶
2) 同时发现的病灶,则病理学恶性程度高的为主病灶;如病理类型相同,则病灶大的,或浸润深度更深的为主病灶
3) 2/3的病例主、副病灶大体类型和组织学类型相同
高危人群和危险因素
丁教授将高危因素概括为:
高龄,男性,胃部腺瘤,家族史[3]
年龄≥65岁为SMEGC独立危险因素[4]
胃窦部,肠上皮化生,原发病灶<lcm为独立危险因素[5]
年龄>60岁,吸烟,OLGIM III/IV[6]
ESD术前精查漏诊原因分析
关于SMEGC漏诊的相关研究:
1)部分SMEGC为内镜治疗时已存在但被遗漏的、术后12个月内经内镜发现的
继发性病灶[7]
2)大阪大学多中心回顾性队列研究: 19% (21/110例)在第一次ESD被遗漏胃部上1/3居多,遗漏率与内镜医师经验缺乏有关 (<500例内镜检查)[8]
3)专家级别的内镜医师也会错过27.5%SMEGC患者的副病灶[7]
治疗策略
丁教授经过文献解析[9],将治疗策略概括为:
1)当肿瘤足够小且手术操作时间<2 h,可以对肿瘤行同时性切除
2) 如果预计手术时间>2h建议行分次切除。若肿瘤恶性程度不同,建议先行恶性程度较高的肿瘤切除
3) 内镜切除后的伤口愈合一般需要4周以上,所以建议两次手术的间隔时间至少为4周
4) 对于不符合ESD标准的SMEGC,可采用先发内镜切除联合手术
文献出处:
[1] Lee H J, Lee Y J, Lee J Y, et al. Characteristics of synchronous and metachronous multiple gastric tumors after endoscopic submucosal dissection of early gastric neoplasm[J]. Clinical Endoscopy, 2018, 51(3): 266-273.
[2] Kim J H, Jeong S H, Yeo J, et al. Clinicopathologic similarities of the main and minor lesions of synchronous multiple early gastric cancer[J]. Journal of Korean medical science, 2016, 31(6): 873-878.
[3] Eom B W, Lee J H, Choi I J, et al. Pretreatment risk factors for multiple gastric cancer and missed lesions[J]. Journal of surgical oncology, 2012, 105(8): 813-817.
[4] Nitta T, Egashira Y, Akutagawa H, et al. Study of clinicopathological factors associated with the occurrence of synchronous multiple gastric carcinomas[J]. Gastric Cancer, 2009, 12: 23-30.
[5] Kodama M, Mizukami K, Hirashita Y, et al. Differences in clinical features and morphology between differentiated and undifferentiated gastric cancer after Helicobacter pylori eradication[J]. Plos one, 2023, 18(3): e0282341.
[6] Brito-Gonçalves G, Libânio D, Marcos P, et al. Clinicopathologic characteristics of patients with gastric superficial neoplasia and risk factors for multiple lesions after endoscopic submucosal dissection in a Western country[J]. GE-Portuguese Journal of Gastroenterology, 2020, 27(2): 76-89.
[7] Lee HL, Eun CS, Lee OY et al. When do we miss synchronous gastric neoplasms with endoscopy? Gastrointest Endosc 2010; 71: 1159–65.
[8] Kato M, Nishida T, Yamamoto K, et al. Scheduled endoscopic surveillance controls secondary cancer after curative endoscopic resection for early gastric cancer: a multicentre retrospective cohort study by Osaka University ESD study group[J]. Gut, 2013, 62(10): 1425-1432.
[9] Kasuga A, Yamamoto Y, Fujisaki J, et al. Simultaneous endoscopic submucosal dissection for synchronous double early gastric cancer[J]. Gastric Cancer, 2013, 16: 555-562.
讲课出处:2020南方消化疾病及消化内镜国际论坛