视频1(EUS视频)
病例 2
多数情况下,IPMN的瘤体在胰管内呈匍匐生长,仅少数成结节样生长,因此上述典型的超声图像反而极少能观察到。接着分享一例临床反而较为常见的IPMN“典型”图像。患者,女性,73岁,患者因“上腹痛三年,检查发现胰管扩张8月”住院。CT 及MRI和MRCP(见 视频 2 图5)可见胰体、尾部主胰管扩张,主胰管内未见明确瘤体,胰头部主胰管正常。
视频2 (CT视频)
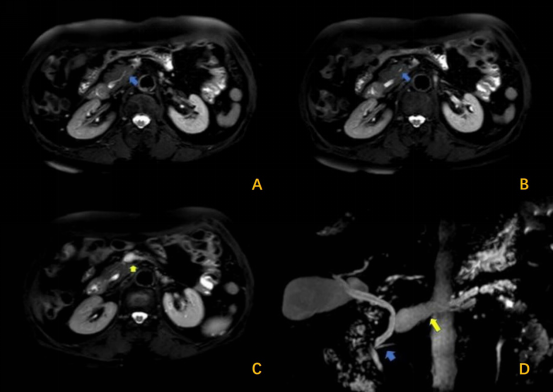
图5:MRI及MRCP图像(黄色箭头:胰体、尾部主胰管扩张;蓝色箭头:胰头部主胰管正常)
EUS胃腔内探查,可见胰体、尾部主胰管扩张,胰头部主胰管正常,正常和扩张主胰管交界处可见可疑瘤体,同时该病人十二指肠主乳头可见腺瘤样增生,但十二指肠乳头腺瘤并未引起胰头部主胰管梗阻、扩张(视频2),对于这类型的IPMN,传统影像学多通过间接征象诊断,但EUS能对十二指肠乳头及胰腺实质的全程探查,进而可以排除十二指肠乳头部位的腺瘤或癌至胆总管、主胰管全程扩张。
视频3(EUS视频)
病例 3
主胰管型IPMN可发生在主胰管的任何部位,病灶如位于胰体尾主胰管时,后方扩张的主胰管及分支胰管,使局部呈多囊性改变,有时较难与黏液性囊腺瘤鉴别,往往需术后病理确诊。遇到上述病例,病灶成结节样阻塞主胰管,EUS探查时从正常主胰管追踪主胰管,在多囊性病灶中分辨真正的主胰管,在扩张的主胰管及正常胰管交界都可发现结节,下面分享一例类似病例。患者,男,65岁,CT、MRI及MRCP均提示胰尾实质萎缩,胰尾部可见多囊性病灶(图 6-7)。
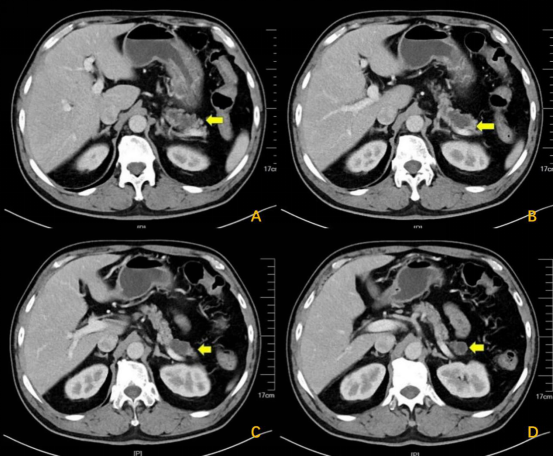
图6:CT图像(黄箭头为多囊性病灶)
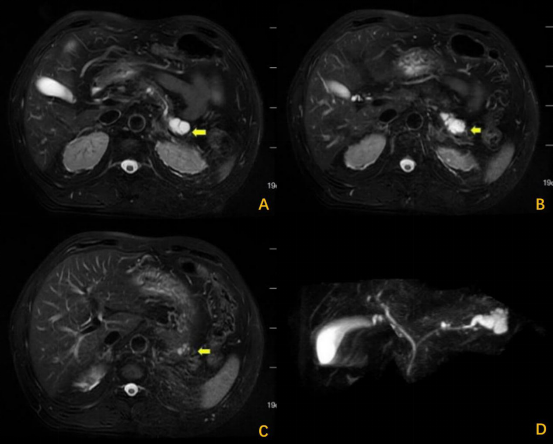
图7:MRI及MRCP图像(黄箭头为病灶)
超声内镜仔细探查,发现扩张的主胰管(黄色箭头)内可见实性结节(绿色箭头),EUS-FNA(橙色箭头)囊液为黏液,CEA异常升高,术后提示主胰管型IPMN(图8和视频4)。
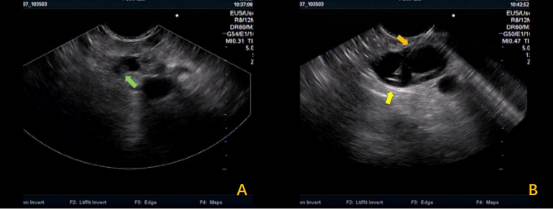
图8:EUS图像(黄箭头:扩张的主胰管,绿箭头:胰管内结节)
视频4(穿刺液)
病例4
最后汇报分支胰管型IPMN的影像学特点,患者,男性,60岁,CT、MRI及MRCP可见胰头部的多囊性病灶(视频5 ,图9)
视频 5(CT)
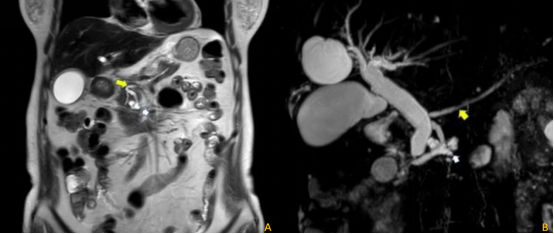
图9:MRI及MRCP图像(黄箭头为主胰管,白箭头为病灶)
及EUS探查见多发分支胰管囊性扩张,呈“葡萄串状”,扩张的胰管内未见明显结节。(视频 6 )
视频 6(EUS视频)
混合胰管型IPMN以上两种影像学特点兼有,但主胰管型IPMN胰管压力较大时,往往分支胰腺管亦囊性扩,此时与混合胰管型IPMN鉴别困难。
IPMN是一类高度异质性胰腺囊性肿瘤,它是以导管内乳头状赘生物生长和粘液分泌为特征的胰腺导管上皮瘤,普遍认为IPMN是一种癌前病变,且常常多发。对于类似IPMN的胰腺囊性肿瘤,MRI及MRCP能提供较多有价值的信息,如有无分隔、分隔厚薄、囊壁有无结节、病灶是否与胰管相通。然而,EUS在附壁结节特别是微小结节的大小判判断上更有优势,并且随着EUS-FNA的广泛应用,不仅能够从影像学特征上判断肿瘤性质和范围,还可以进一步获取肿瘤的细胞学和组织学信息,为后续治疗策略的选择提供更多依据。
作者丨程桂莲,吴伟,徐丽明,胡端敏
来源丨苏州大学附属第二医院消化科
随着医学影像学技术的发展,胰腺囊性疾病(Pancreas cystic lesions PCLs)的检出率逐年增加,对于这类疾病的认识也日益提高,胰腺囊性疾病是指由胰腺上皮和(或)间质组织形成的肿瘤或非肿瘤性(单发或多发的肿瘤样)含囊腔的病变,其中胰腺囊性肿瘤(pancreatic cystic neoplasms,PCNs)尤其受到临床医生的关注,PCNs临床上分类众多,以浆液性囊腺瘤、黏液性囊腺瘤、导管内乳头状黏液性肿瘤、实性假乳头状瘤四种囊性肿瘤最多见(图1)。
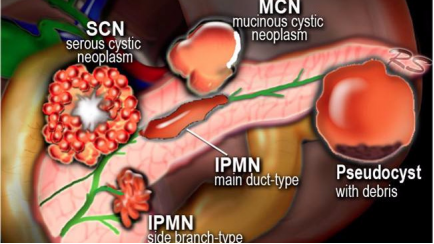
图1:不同的胰腺囊性疾病
各类PCNs性质不一,癌变率也存在较大差异。因此,准确的定性诊断对治疗策略的选择意义重大。不同囊性肿瘤虽有各自好发年龄及影像学特点,但对于不典型病例的鉴别诊断仍是临床难题。EUS借助其高分辨探头和近距离探查的优势,可细致观察囊肿内部结构特征,能清楚的分辨病灶与胰管的关系,同时结合细针穿刺抽吸囊液,为胰腺囊性肿瘤的鉴别诊断提供详实有力的证据。本期微信主要通过四个病例与大家分享胰腺囊性肿瘤中相对比较常见的胰腺导管内乳头状黏液性肿瘤(Intraductal Papillary Mucinous Neoplasm,IPMN)的超声内镜图像。
IPMN是良性到交界性乃至浸润性癌演变的疾病。病理表现为胰腺导管上皮肿瘤在胰管内生长并分泌大量黏液造成主胰管和(或)分支胰管的囊性扩张、胰腺实质的萎缩,多数肿瘤成纵行匍匐生长,少数可呈结节样生长。按肿瘤位于胰管内的部位将其分为主胰管型、分支胰管型及混合型IPMN。
病例 1
首先介绍一例典型的主胰管型IPMN病例的EUS图像。患者男性,80岁,因“脂肪泻一月”住院,患者CT、MRI及MRCP均见胰腺萎缩,主胰管全程扩张(图2-3),符合主胰管型IPMN的影像学特点,但主胰腺内未见明显的结节。
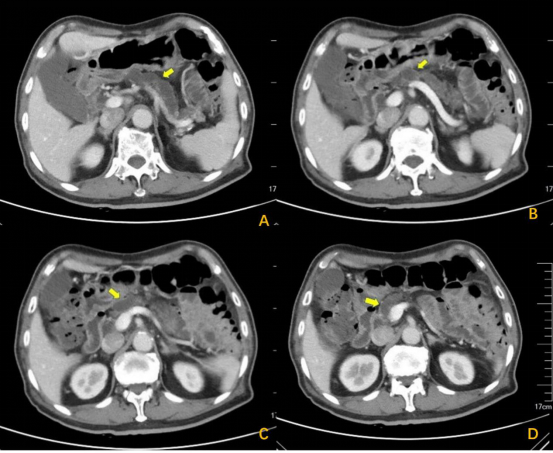
图2:CT (黄色箭头为全程扩张胰管)
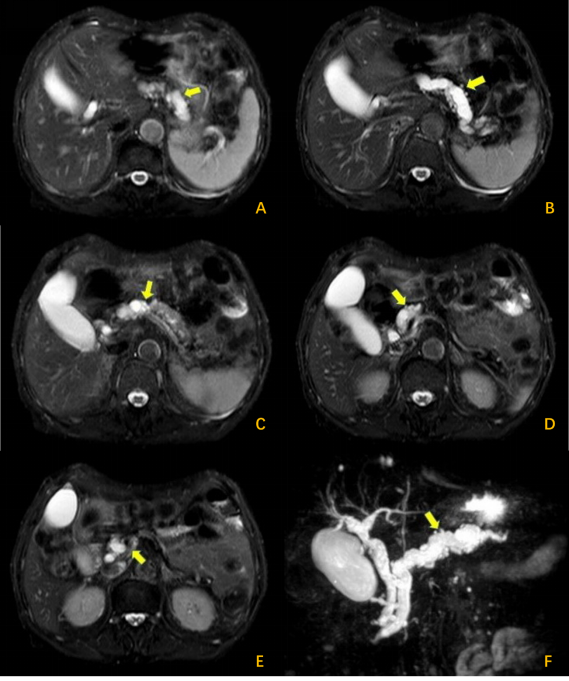
图3:MRI及MRCP(黄色箭头为全程扩张胰管)
超声内镜于胃腔内探查见胰腺实质萎缩,主胰管全程扩张,在胰颈部主胰管内见结节样低回声病变(图4 A),探头进入降部,白光下见到IPMN最典型的表现,十二指肠乳头被透明胶冻样物体附着(见图4 B),诊断主胰管型IPMN。(见视频1)
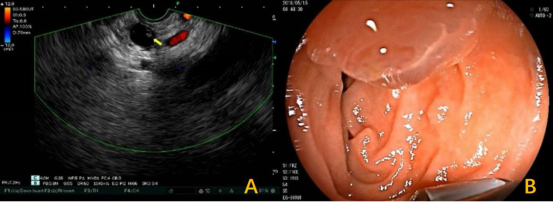
图4:A:EUS见胰管内结节(黄色箭头)B:白光下十二肠乳头
视频1(EUS视频)
病例 2
多数情况下,IPMN的瘤体在胰管内呈匍匐生长,仅少数成结节样生长,因此上述典型的超声图像反而极少能观察到。接着分享一例临床反而较为常见的IPMN“典型”图像。患者,女性,73岁,患者因“上腹痛三年,检查发现胰管扩张8月”住院。CT 及MRI和MRCP(见 视频 2 图5)可见胰体、尾部主胰管扩张,主胰管内未见明确瘤体,胰头部主胰管正常。
视频2 (CT视频)

图5:MRI及MRCP图像(黄色箭头:胰体、尾部主胰管扩张;蓝色箭头:胰头部主胰管正常)
EUS胃腔内探查,可见胰体、尾部主胰管扩张,胰头部主胰管正常,正常和扩张主胰管交界处可见可疑瘤体,同时该病人十二指肠主乳头可见腺瘤样增生,但十二指肠乳头腺瘤并未引起胰头部主胰管梗阻、扩张(视频2),对于这类型的IPMN,传统影像学多通过间接征象诊断,但EUS能对十二指肠乳头及胰腺实质的全程探查,进而可以排除十二指肠乳头部位的腺瘤或癌至胆总管、主胰管全程扩张。
视频3(EUS视频)
病例 3
主胰管型IPMN可发生在主胰管的任何部位,病灶如位于胰体尾主胰管时,后方扩张的主胰管及分支胰管,使局部呈多囊性改变,有时较难与黏液性囊腺瘤鉴别,往往需术后病理确诊。遇到上述病例,病灶成结节样阻塞主胰管,EUS探查时从正常主胰管追踪主胰管,在多囊性病灶中分辨真正的主胰管,在扩张的主胰管及正常胰管交界都可发现结节,下面分享一例类似病例。患者,男,65岁,CT、MRI及MRCP均提示胰尾实质萎缩,胰尾部可见多囊性病灶(图 6-7)。

图6:CT图像(黄箭头为多囊性病灶)

图7:MRI及MRCP图像(黄箭头为病灶)
超声内镜仔细探查,发现扩张的主胰管(黄色箭头)内可见实性结节(绿色箭头),EUS-FNA(橙色箭头)囊液为黏液,CEA异常升高,术后提示主胰管型IPMN(图8和视频4)。

图8:EUS图像(黄箭头:扩张的主胰管,绿箭头:胰管内结节)
视频4(穿刺液)
病例4
最后汇报分支胰管型IPMN的影像学特点,患者,男性,60岁,CT、MRI及MRCP可见胰头部的多囊性病灶(视频5 ,图9)
视频 5(CT)

图9:MRI及MRCP图像(黄箭头为主胰管,白箭头为病灶)
及EUS探查见多发分支胰管囊性扩张,呈“葡萄串状”,扩张的胰管内未见明显结节。(视频 6 )
视频 6(EUS视频)
混合胰管型IPMN以上两种影像学特点兼有,但主胰管型IPMN胰管压力较大时,往往分支胰腺管亦囊性扩,此时与混合胰管型IPMN鉴别困难。
IPMN是一类高度异质性胰腺囊性肿瘤,它是以导管内乳头状赘生物生长和粘液分泌为特征的胰腺导管上皮瘤,普遍认为IPMN是一种癌前病变,且常常多发。对于类似IPMN的胰腺囊性肿瘤,MRI及MRCP能提供较多有价值的信息,如有无分隔、分隔厚薄、囊壁有无结节、病灶是否与胰管相通。然而,EUS在附壁结节特别是微小结节的大小判判断上更有优势,并且随着EUS-FNA的广泛应用,不仅能够从影像学特征上判断肿瘤性质和范围,还可以进一步获取肿瘤的细胞学和组织学信息,为后续治疗策略的选择提供更多依据。