程桂莲 吴伟 徐丽明 胡端敏
苏州大学附属第二医院 消化科
纵隔是左右纵隔胸膜之间的器官、结构和结缔组织的总称。纵隔呈矢状位,位于胸腔正中偏左,上窄下宽,前短后长。纵隔的前界为胸骨,后界为脊柱,两侧为纵隔胸膜。纵隔内有心脏、大血管、食管、气管、神经、胸腺、胸导管、丰富的淋巴组织和结缔脂肪组织。为了便于标明病变在纵隔内的所在部位,可将纵隔划分为若干部分。简单的划区法是以胸骨角与第4胸椎下缘的水平连线为界,把纵隔分成上纵隔及下纵隔,其中下纵隔又分为前、中、后纵隔(如图1)。
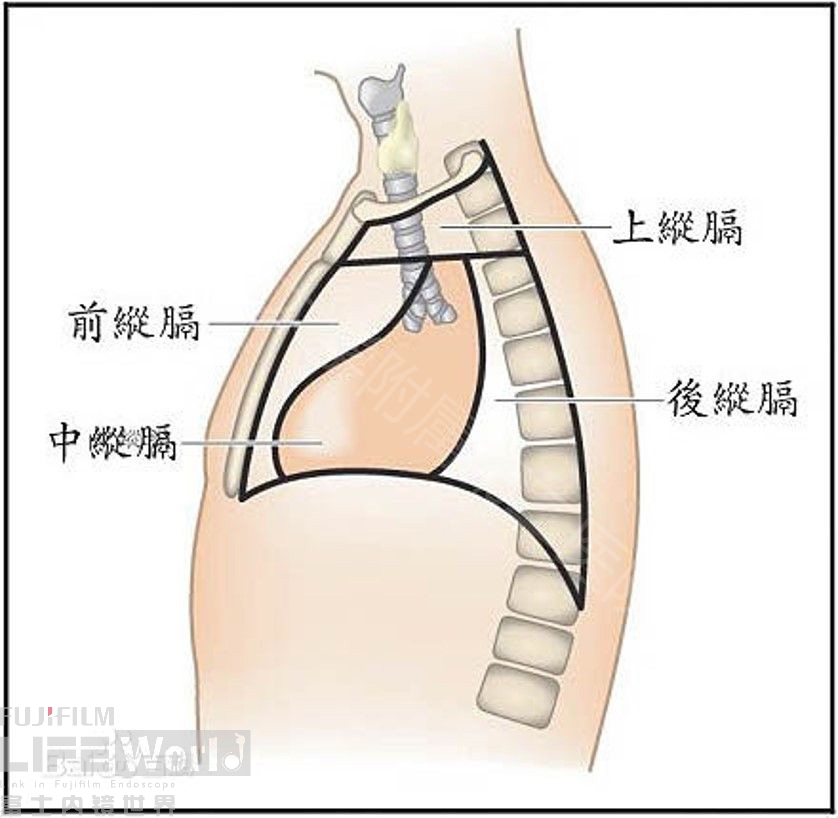
图1:纵隔示意图
纵隔疾病是临床常见的一组疾病,包括胸腺瘤、纵隔囊肿、结节病等良性疾病,以及恶性疾病如纵隔恶性肿瘤、淋巴瘤、各种癌症纵隔淋巴结转移等。纵隔疾病的组织的获取至关重要,主要活检手段包括:内窥镜技术(支气管镜);放射学方法引导(CT及MRI),外科手术活检(纵隔镜及可视化胸腔镜)。而超声衍生技术(EUS及EUBS)的发展,改变了纵隔疾病评估的流程,同时逐步取代了其他方式成为纵隔疾病活检的首选方式。国际肺癌研究协会(IASLC)将纵隔淋巴结分为14个区域,超声内镜(Endoscopic Ultrasound ;EUS)及超声支气管镜 (Endobroncheal Ultrasonography; EBUS) 可覆盖所有站点的淋巴结(图2)。
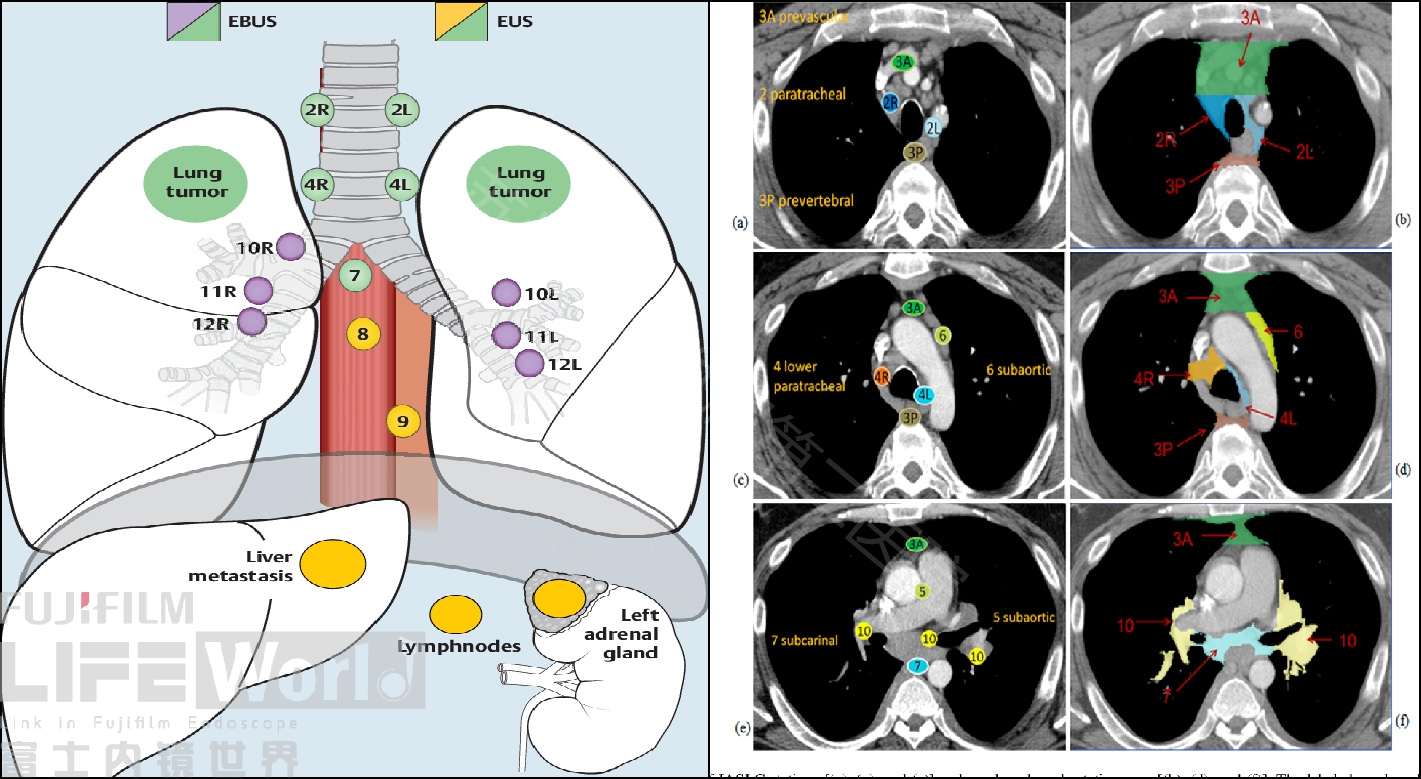
图2 国际肺癌研究协会(IASLC)纵隔淋巴结分区
A: EUS和EBUS覆盖区域 黄色球(仅EUS)、紫色球(仅EBUS)、绿色球(EUS和EBUS均能)B: CT上的各区域淋巴结
由此可见,超声内镜引导下穿刺活检术可覆盖纵隔所有区域疾病的活检,但纵隔内有重要脏器及大血管,穿刺活检风险大,常见的并发症有出血、感染、气胸及呼吸衰竭等(其中气胸及呼吸衰竭常见于EBUS引导下穿刺术)。而最大程度避免并发症的要点为熟知纵隔解剖及探查技巧。
第一部分:纵隔的探查技巧
对于任何部位EUS的探查,第一步均在白光下找到起点,即进镜至胃腔,白光下寻找起点(肝左叶),此时顺时针旋转180°,沿途能观察到肝左、肝中及肝右静脉汇入下腔静脉(见前期腹主动脉及重大分支的EUS探查技巧),追寻下腔静脉逐步退镜,可见下腔静脉汇入右心房,稍退镜及左旋镜身即可见上下腔静脉汇入右心房,同时左心房位于右心房与探头之间或靠近头侧(图3A),在该平面,稍左旋镜身,可观察到左心房与左心室间的二尖瓣,左心室流出道、主动脉瓣,左冠状动脉及肺动脉主干(图3B、C)。主动脉根部的直径为2.4-4.7厘米(男性比女性大),位于右心室流出道后的左心室底部,主动脉很宽,有三个扩张,称为冠脉窦(右冠脉窦-右前,左冠脉窦-左后和无冠脉窦-右后)(图3D)。继续退镜,可显示左心房头侧的右肺动脉(呈一类圆形切面)(图3E),微调镜身,可见右肺动脉为肺动脉干延续并与主动脉交叉走形。此区域为气管隆嵴(气体回声),于气管隆嵴下区域左右旋转45°分别可见左右主支气管(振铃声像)(图3F),右旋镜身可见右侧肺门(图3G),左旋镜身可见左肺动静脉,显示左肺动脉后退镜在图像头侧可见主动脉弓,在肺动脉与主动脉弓区域为主肺动脉窗(AP 窗)(图3H),AP窗内可见动脉韧带,如有动脉导管未闭,在此区域可见血流信号。主动脉弓平面稍退镜及旋转镜身,左旋过程中分别可见左颈总动脉及左锁骨下动脉(图3I),左侧头臂干在气管的前方无法观察,沿着颈总动脉逐步退镜可见左颈内静脉伴随颈总动脉上行(图3J)。在主动脉弓平面右旋可显示升主动脉横断面,左旋可显示降主动脉起始段,沿着降主动脉进镜(降主动脉平行于食道走形,图3K)超声图上以长轴显示,在降主动脉平面,左旋45°左右,可见奇静脉(图3L),沿着奇静脉向头侧扫查,可见奇静脉汇入上腔静脉(视频1)。
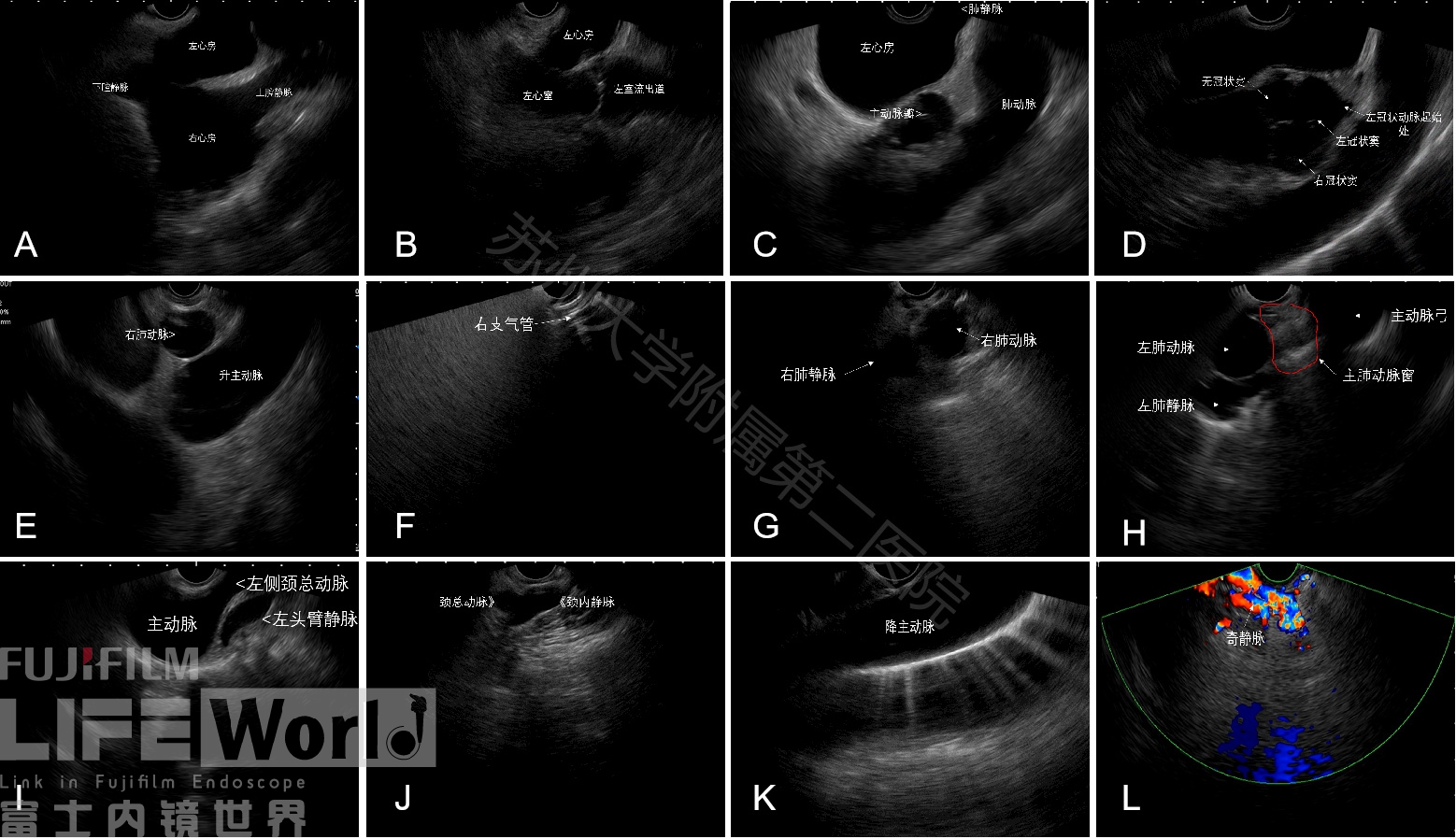
图3:线阵EUS纵隔探查步骤
视频1
第二部分:纵隔常见疾病的EUS表现
纵膈疾患较多,但需要EUS-FNA协助诊断的主要是肿大淋巴结。纵隔淋巴结肿大的原因复杂,恶性病变有:淋巴瘤、巴结转移癌等;良性则包括:结核、结节病、巨淋巴结增生症、慢性淋巴结炎等,首先跟大家分享恶性淋巴结肿大的EUS声像特点。
(一)恶性淋巴结肿大
恶性淋巴结肿大最常见病因有肺癌或食管癌伴淋巴转移,其中原发性肺癌或肺癌术后复发伴纵隔淋巴结转移多见,EUS影像有以下几点:类圆形、均匀低回声、直径大于1cm、淋巴门结构消失,具体病例如下:
病例一:老年患者,肺癌术后6年,CT发现纵膈占位。EUS可见纵隔多发肿大淋巴结,其EUS声像符合恶性淋巴表现,进一步行EUS-FNA穿刺,术后病理低分化恶性肿瘤,伴神经内分泌化(图4)。
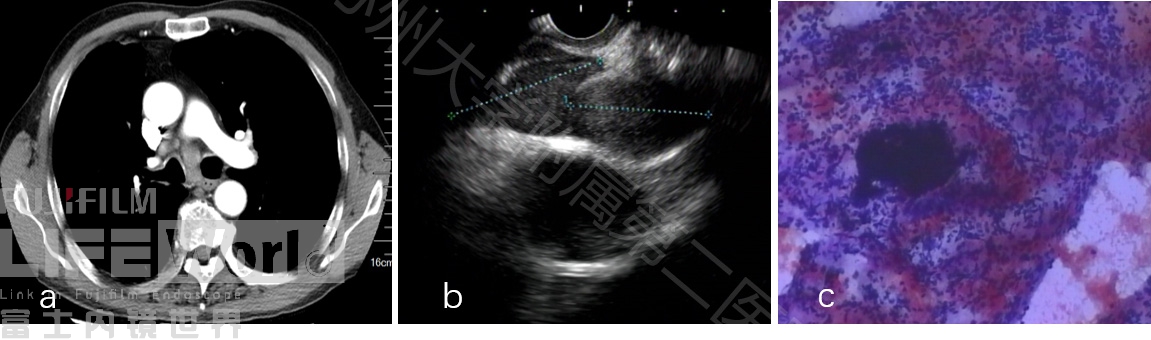
图4 右气管旁淋巴结(第4R站)
病例二: 老年女性,胸痛半月入院,PET提示右肺下叶结节灶,纵隔,腹膜后多发肿大淋巴结。EUS隆突下见多发肿大淋巴结,FNA结果腺癌,结合免疫标记考虑肺来源(图5)。
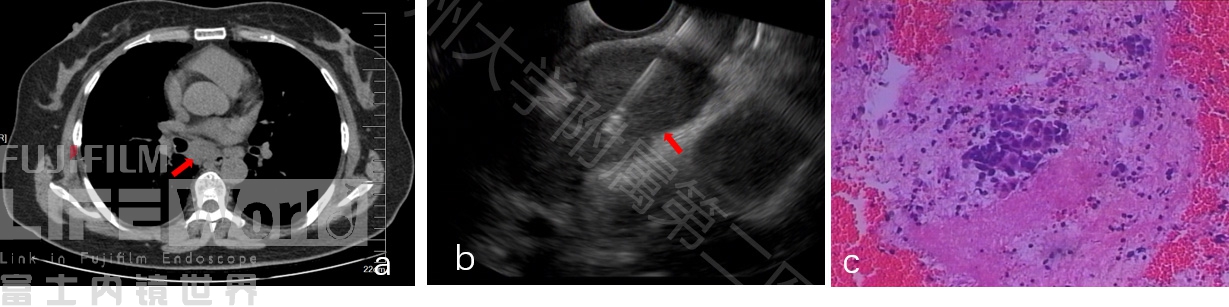
图5 隆突下淋巴结(第7站)
除肺癌外,其次为食管癌伴纵隔淋巴结转移,胃镜可发现食管晚期肿瘤表现,但我们工作碰到了一例较少见的粘膜光滑的进展期食管癌伴纵隔多发转移,具体情况如下:
病例三、中年女性,因上腹不适、消瘦行胃镜检查,镜下见食道多发粘膜下隆起灶,表面粘膜光滑,CT发现食道壁增厚,纵隔、腹盆腔多发肿大淋巴结,初诊考虑淋巴瘤,进一步行EUS检查,见食道粘膜下层明显增厚,纵隔多发肿大淋巴结,符合恶性淋巴结特点(类圆形、均匀低回声、直径大于1cm、淋巴门结构消失),FNA穿刺结果显示:食道鳞状细胞癌,纵隔淋巴结及腹膜后淋巴结转移性鳞癌(图6)。
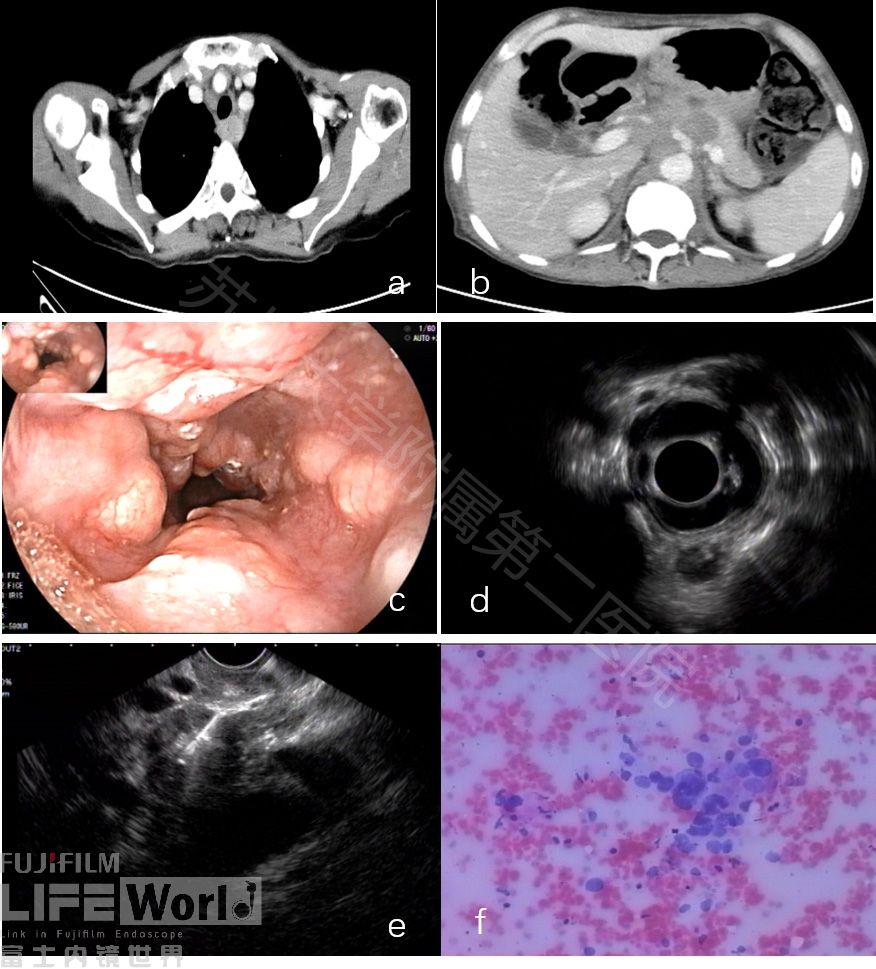
图6 (a和b:CT图;c:内镜图;d和e:环扫和线阵EUS;f:细胞涂片)
此外,淋巴瘤是纵隔淋巴结病变的另一原因。在EUS上,淋巴结肿大成均质、低回声,有时伴有内部无回声坏死区,甚至融合成片。既往观念认为FNA取材有限导致淋巴瘤诊断困难。近年,各种穿刺方法及穿刺针等的改革,尤其是EUS-FNB针的使用使得样本量明显增加,从而可以做到淋巴瘤亚分类。
(二)良性淋巴结肿大
良性疾病亦可导致纵隔淋巴结肿大,其中淋巴结结核多见,纵隔淋巴结结核分为原发性和继发性两种,原发性病因不明,表现为慢性肉芽肿,继发性多由邻近部位结核感染波及,多来自于肺结核。继发性肺结核常存在典型的纵隔外结核证据,因此不难诊断,相对而言,原发性纵隔淋巴结结核诊断较为困难。如临床上遇到青少年男性,孤立纵隔肿大淋巴结需高度怀疑淋巴结结核。
病例四:青年男性,胸骨后痛入院,CT提示后纵隔占位,胃镜提示食管隆起(外压),穿刺病理提示淋巴细胞多克隆增生,术后病理提示肉芽肿性炎性坏死,考虑结核。
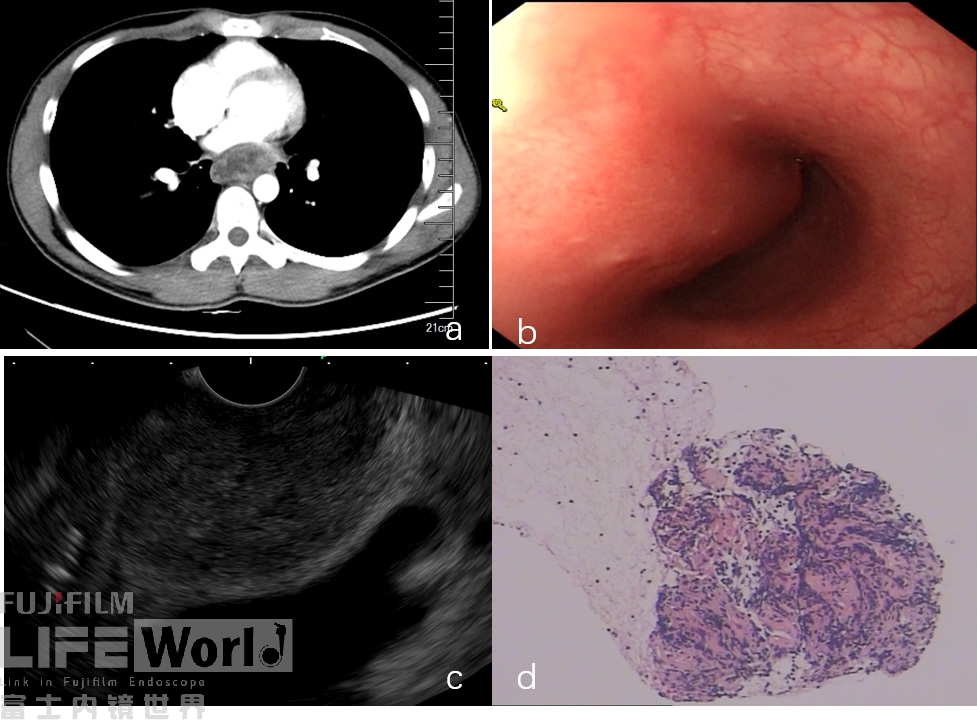
图7 纵隔淋巴结结核
病例五:老年女性,体检发现纵隔淋巴结肿大,无不适。EUS探查见纵隔巨大淋巴结,但呈三角形,中央可见高回声淋巴门结构,两次穿刺均提示淋巴多克隆增生,后证实结节病,目前随访中。
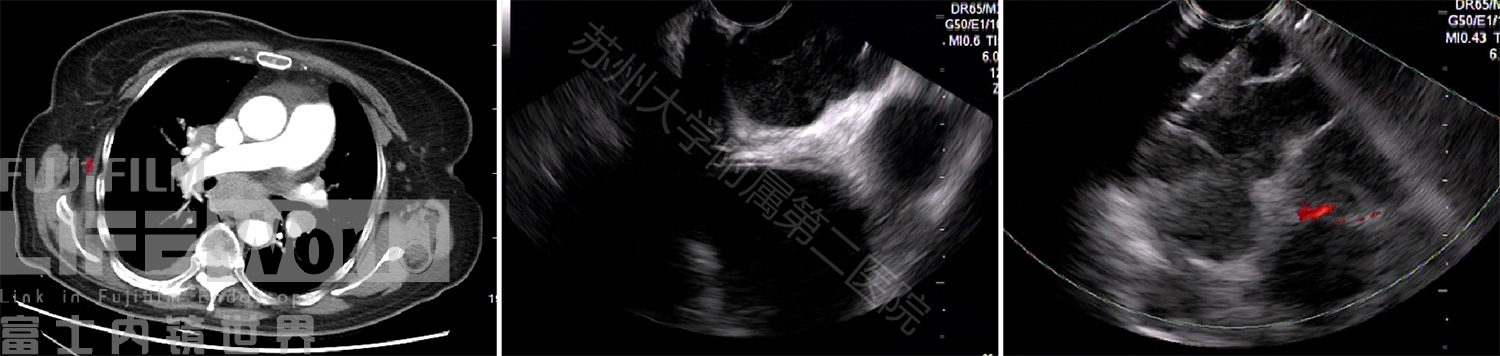
图8 肺结节病
细菌、病毒、衣原体、真菌等引起的急慢性淋巴结感染,淋巴结可充血水肿,淋巴细胞和巨噬细胞增生、中性粒细胞、单核细胞及浆细胞的浸润,甚至发生坏死及肉芽肿形成。如肿大淋巴结位于浅表,则常伴有疼痛,对症治疗即可使肿大的炎症性淋巴结缩小。本中心即遇到一例EB病毒感染导致的淋巴结肿大。
病例六:中年女性,胸闷咳嗽一月,发现纵隔多发肿大淋巴结,穿刺(胸主动脉水平)病理提示淋巴组织增生性病变,EBV病毒阳性,对症处理后好转出院。
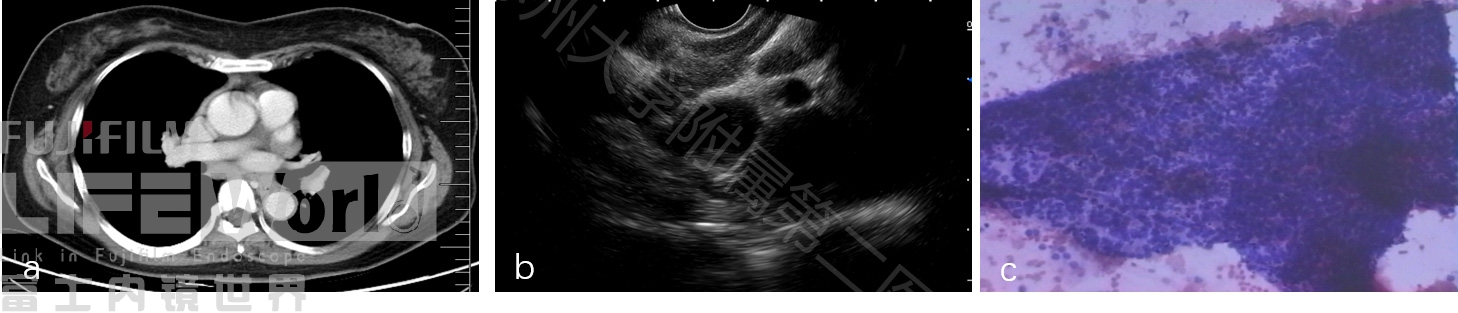
图9 EB病毒感染
(三)其他纵膈疾病
纵隔疾病除了肿大淋巴结,还有原发纵隔的肿瘤,其病变性质与起源器官和周围结构有关。其中畸胎瘤和囊肿、胸腺瘤、胸内甲状腺瘤等常见于前纵隔,气管囊肿、食管囊肿、囊状淋巴瘤、淋巴瘤、其他部位肿瘤的转移淋巴结等多见于中纵隔,神经源性肿瘤常见于后纵隔。下面这一病例即为支气管囊肿。
病例七:中年男性,体检发现中后纵隔占位,EUS发现气管分叉附近见巨大囊实性占位,MRI提示支气管囊肿,手术病理提示支气管囊肿伴囊壁肌肉组织增生。
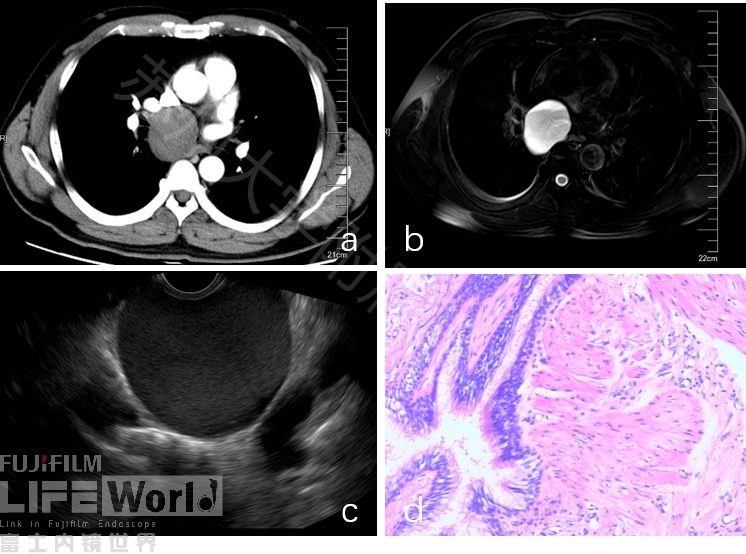
图10 支气管囊肿
病例八:任何部位的晚期肿瘤都可出现纵隔转移,如卵巢癌、结直肠癌、胰腺癌等。下面患者卵巢癌术后十年,近半年开始出现进行性进食哽噎感,X-线钡餐示食道下段呈“鸟嘴样”改变,考虑贲门失弛缓,拟行POEM手术入院,术前超声胃镜探查发现局部食道壁明显增厚,代之弥漫增厚低回声改变,与贲门失弛缓征象不符,故行EUS-FNA术。最终FNA病理提示低分化腺癌,免疫标记提示卵巢来源(图 11-12)。
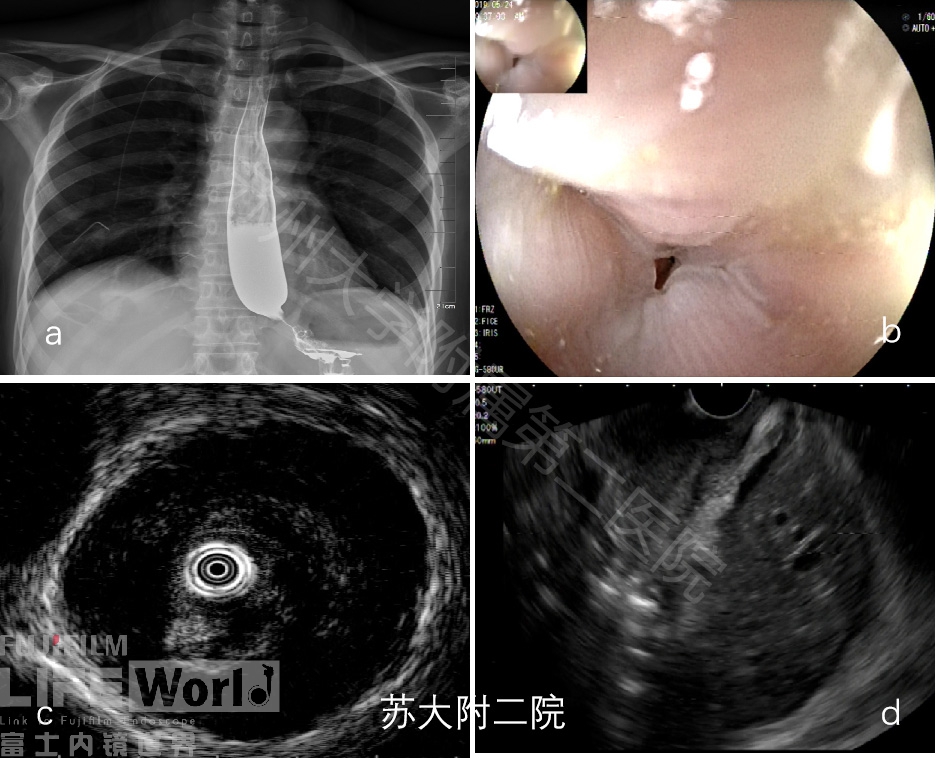
图11: a X-线钡餐显示 “鸟嘴征”; b 胃镜下局部粘膜光滑,管腔狭窄;c EUS声像 d EUS-FNA)
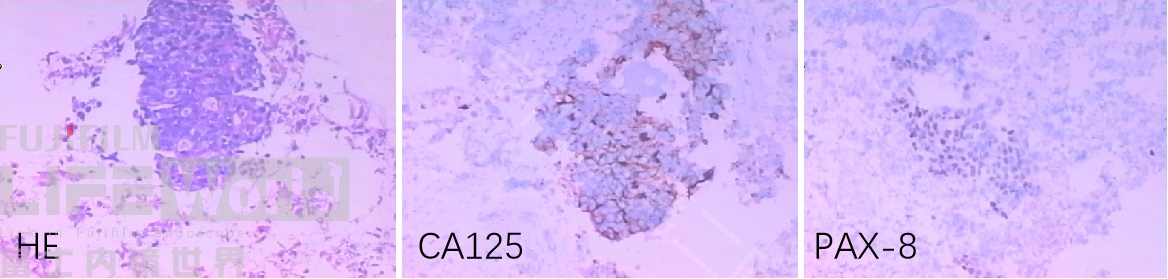
图12(免疫病理)
病例九 食道紧邻心脏及纵隔大血管,这种解剖优势早已被应用于临床,如经食道的超声心动图(transesophageal echocardiogram (TEE))。Kinza等[1]人在一项前瞻性研究中证实了EUS可以很好的评估二尖瓣、主动脉瓣、主动脉、心包和左心室功能,在紧急情况下可以作为一种有用的早期诊断工具。我们就曾在EUS常规探查时意外发现心包积液患者,后证实为肺癌心包转移。
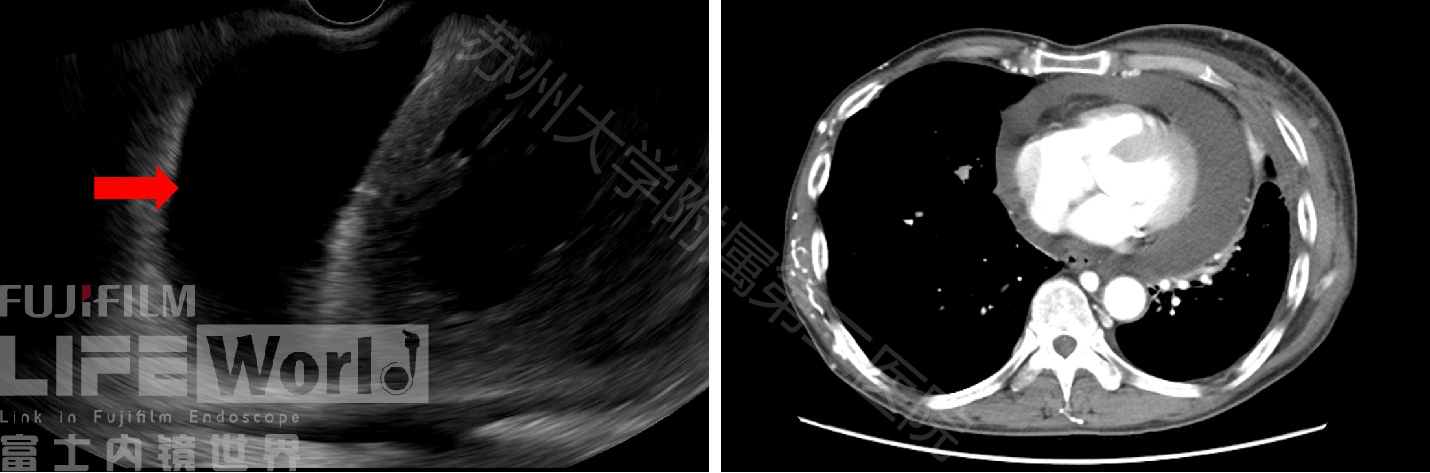
图13:心包积液A:EUS表现(红箭头)B:相应的CT图
Fritscher等[2]人在一项存活猪研究中,在EUS引导下成功穿刺心脏进入左心房、左心室、冠状动脉,术中术后无不良事件报道;随后是三个临床病例,其中两例做了心包积液穿刺引流,一例为左心房肿块穿刺活检,同样无不良事件报道(图25)。随即,EUS引导下的右心房肿块和心包肿瘤也陆续有报道[3、4]。
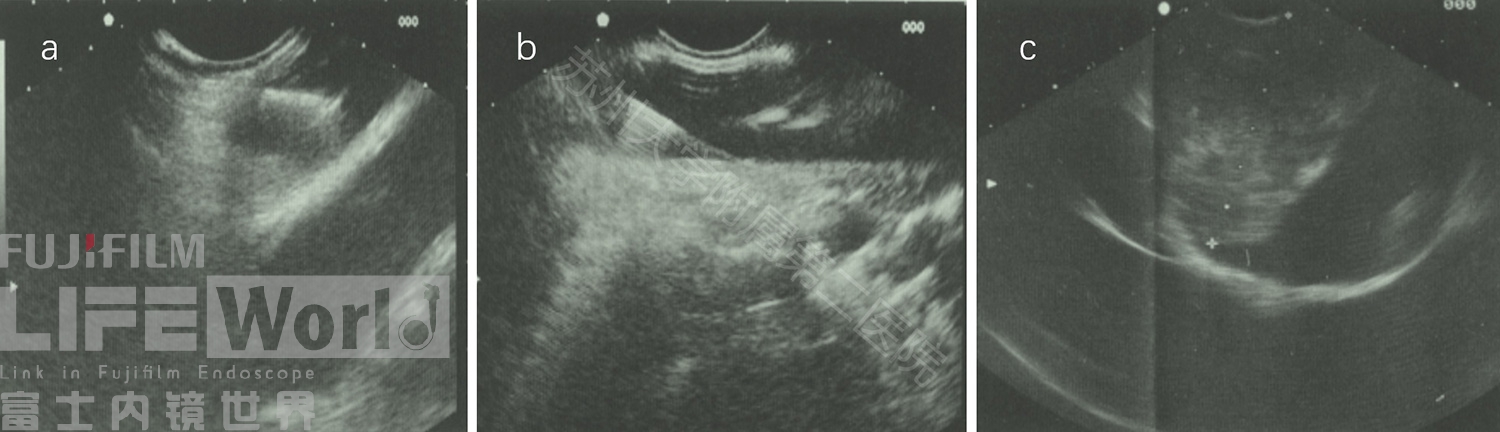
图14(a EUS引导下左心室穿刺;b EUS引导下穿刺冠状动脉 c EUS引导下左心房肿块活检术 图片来源于Fritscher-Ravens A, Ganbari A, Mosse CA, et al. Transesophageal endoscopic ultrasound‑guided access to the heart. Endoscopy 2007;39:385‑9)
纵隔疾病,由于其病种繁多、与重要脏器及血管紧密相连且活检困难,一向是临床医师诊断难点。EUS可清晰显示食管周围的中、后纵隔病变,可明确病变与正常纵隔器官间的解剖关系,最重要的是可以避开重要结构,对病灶进行实时监测下的活检。超声内镜在纵隔内应用主要包括两部分:肺癌的诊断及分期、纵隔肿块或肿大淋巴结的组织活检。如前所诉,EUS及EBUS的联合可覆盖所有站点淋巴结,最近国际肺癌分期指南提出超声内镜应作为肺癌淋巴结分期的首选活检方式。 EUS-FNA相对于EBUS-TBNA而言,具有更好的患者耐受性、手术耗时短以及呼吸系统并发症少的优势。因而,介于EUS及EBUS均能介入的淋巴结,临床上更倾向于选择EUS。同时肝脏及肾上腺也是肺癌常见转移器官,EUS对于肝脏微小病灶的发现及肾上腺穿刺的可行性保证了肺癌纵隔外转移灶的确认。
超声内镜检查过程中,发现边界清晰,直径大于1cm,呈均匀低回声改变类圆形的淋巴结,需警惕恶性淋巴结。但是,同时具备以上三点特征的毕竟不多,对于无法区分良恶性淋巴结的前提下均推荐FNA。EUS-FNA还适用于以下情况:包括淋巴瘤、结节病、反应性淋巴结、纵隔脓肿、纵隔囊肿、神经源性肿瘤和侵犯纵隔的甲状腺肿瘤。总之,EUS-FNA是一种灵敏、准确、快速、安全且微创的方法,有助于对食管纵隔/肺部病变组织学诊断。
参考文献:
1)Kinza Sentissi, Mandeep S, Sawhney, et al. The Use of Standard Gastrointestinal Endoscopic Ultrasound to Assess Cardiac Anatomy.GI Endoscope and Cardiac Anatomy. 2016; 123:547-550.
2)Fritscher-Ravens A, Ganbari A, Mosse CA, et al. Transesophageal endoscopic ultrasound‑guided access to the heart. Endoscopy 2007;39:385‑9.
3)Romero-Castro R, Rios-Martin JJ, Gallego-Garcia de, et al. Pericardial tumor diagnosed by EUS‑guided FNA (with video). Gastrointest Endosc 2009;69:562‑3
4)Gornals JB, de la Hera M, de Albert M, et al.. EUS cardiac puncture‑guided right atrial tumor. Gastrointest Endosc 2015; 82:165.